




















КАРБОНАРИЙ, КАРБОНАР м tar. karbonari (XIX əsrdə İtaliyada yadellilərin zülmünə qarşı və İtaliyanı birləşdirmək uğrunda mübarizə aparan gizli inqilabi
Tam oxu »[ital. carbonaro] XIX əsrin əvvəllərində İtaliyada meydana gəlmiş, yadellilərin zülmünə qarşı və İtaliyanın birləşməsi uğrunda mübarizə aparan gizli c
Tam oxu »КАРБОНАРИЙ, КАРБОНАР м tar. karbonari (XIX əsrdə İtaliyada yadellilərin zülmünə qarşı və İtaliyanı birləşdirmək uğrunda mübarizə aparan gizli inqilabi
Tam oxu »сущ. карбонарий (член тайного общества, организованного в Италии в начале XIX в. для борьбы против чужеземного гнета, за объединение Италии)
Tam oxu »[ital. carbonaro] XIX əsrin əvvəllərində İtaliyada meydana gəlmiş, yadellilərin zülmünə qarşı və İtaliyanın birləşməsi uğrunda mübarizə aparan gizli c
Tam oxu »-а; м. (от лат. carbo (carbonis) - уголь); хим. 1) Соль угольной кислоты (сода, поташ и др.) 2) геол. Название минералов, представляющих углекислые соединения различных металлов.
Tam oxu »[lat.] карбонат (1. хим. карбондин кьел (сода, поташ ва мс.); 2. хим. геол. карбонат квай минералрин тӀвар; 3. хуьс. чӀулав алмас).
Tam oxu »м karbonat (1. kim. karbonat turşusunun duzu; 2. miner. karbon turşusu olan minerallar; 3. miner. qara almaz).
Tam oxu »хим. I сущ. карбонат: 1. соль угольной кислоты (сода, поташ и др.) 2. название минералов, содержащих углекислоту 3. черный алмаз мелкозернистого строе
Tam oxu »[lat.] 1. kim. Karbon turşusu duzu (soda, potaş və s). 2. kim. geol. Tərkibində karbon turşusu olan mineralların adı. 3. xüs. Xırda dənəli qara almaz
Tam oxu »прил. kim. karbonat; углекислый кадий kalium-karbonat; ◊ углекислый газ karbon qazı; углекислые соли karbonatlar.
Tam oxu »-я; м. (итал. carbonaro) Член тайного общества в Италии в начале 19 в., которое боролось за национальную независимость и воссоединение Италии.
Tam oxu »[fr.] сущ. картонаж (картондикай расай куьлуь затӀар); // картонаждин, картондикай куьлуь затӀар расдай (мес. кархана).
Tam oxu »-а; м. см. тж. картонажный а) Изделие из картона, картонажное изделие. Клеить картонажи. б) лекс., собир. Мастерская картонажа.
Tam oxu »I сущ. картонаж (небольшое изделие из картона) II прил. картонажный. Kartonaj emalatxanası картонажная мастерская, kartonaj məmulatı картонажные издел
Tam oxu »прил. углеродистый. Karbonlu polad тех. углеродистая сталь, karbonlu birləşmələr хим. углеродистые соединения
Tam oxu »I сущ. хим. карбониль (соединение металлов с окисью углерода) II прил. карбонильный Karbonil dəmiri тех. карбонильное железо, karbonil korroziyası кар
Tam oxu »s. cardboard articles pl.; ~ fabrikası factory of cardboard articles; ~ məmulatı cardboard articles
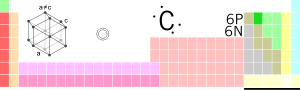
Tam oxu »...tərkib hissəsi olan kimyəvi element. Radioaktiv karbon. Sulu karbon. – Canlının bədənini təşkil edən kimyəvi elementlər içərisində mühüm yer tutan el
Tam oxu »...важнейшая составная часть всех органических веществ). Radioaktiv karbon радиоактивный углерод II прил. 1. углеродный. Karbon birləşmələri углеродные
Tam oxu »






















