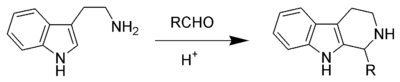
Favorski reaksiyası
Favorski reaksiyası - termiki alkinlərin karbonil qrupuna birləşməsi ilə 1 əvəz olunmuş propargil spirtlərinin sintezi üsuludur. Aleksey Favorski tərəfindən 1905-ci ildə fenil asetilenin ketonlarla kalium hidroksid iştirakı ilə qarşılıqlı təsirini öyrənərkən aşkar etmişdir [1] [2].
:
== Reaksiya mexanizmi ==
Reaksiya, 1-terminal alkinin asetilen anionunun karbonil qrupuna nükleofil əlavə edilməsi mexanizminə görə davam edir:
R
1
R
2
C
=
O
+
R
C
≡
C
−
→
R
1
R
2
C
(
O
−
)
C
≡
C
R
,
R
=
H
,
A
l
k
,
A
r
,
O
E
t
{\displaystyle {\mathsf {R^{1}R^{2}C{\text{=}}O+RC\equiv C^{-}\rightarrow R^{1}R^{2}C(O^{-})C\equiv CR,\ \ R=H,Alk,Ar,OEt}}}
Reaksiya ümumiyyətlə kalium hidroksid və ya natrium amidin həlledicidə (efir, benzol, dimetilformamid və s.) -70 ilə + 40 °C arasında olan temperaturda, az qaynayan birləşmələr və ya asetilen istifadə olunduqda - təzyiq 0.4-0, 9 MPa.təzyiqdə aparılır. Bəzi dəyişikliklərdə asetilen əvəzinə kalium hidroksidin iştirakı ilə kalsium karbid (asetilenid) istifadə olunur.
Məhsullar 40-60% -dir.
Ketonlar və bəzi aldehidlər reaksiyaya girir; alkin komponenti olaraq hər ikisi ilə əvəz olunmuş termik alkinlər (hetero-əvəzlənmişlər, məsələn etoksiasetilen [3] daxil olmaqla) və asetilen istifadə olunur. Sonuncu vəziyyətdə, meydana gələn 1,1-əvəzlənmiş propargil spirtlərinin deprotonlaşdırılması və onların karbonil birləşməsi, bis-adduktlar, asetilenik 1,4-diollarla qarşılıqlı təsiri nəticəsində də meydana gələ bilər:
R
1
R
2
C
=
O
+
H
C
≡
C
−
→
R
1
R
2
C
(
O
−
)
C
≡
C
H
{\displaystyle {\mathsf {R^{1}R^{2}C{\text{=}}O+HC\equiv C^{-}\rightarrow R^{1}R^{2}C(O^{-})C\equiv CH}}}
R
1
R
2
C
(
O
−
)
C
≡
C
H
+
B
−
→
R
1
R
2
C
(
O
−
)
C
≡
C
−
+
B
H
{\displaystyle {\mathsf {R^{1}R^{2}C(O^{-})C\equiv CH+B^{-}\rightarrow R^{1}R^{2}C(O^{-})C\equiv C^{-}+BH}}}
R
1
R
2
C
(
O
−
)
≡
C
−
+
R
1
R
2
C
=
O
→
R
1
R
2
C
(
O
−
)
C
≡
C
(
O
−
)
R
1
R
2
{\displaystyle {\mathsf {R^{1}R^{2}C(O^{-})\equiv C^{-}+R^{1}R^{2}C{\text{=}}O\rightarrow R^{1}R^{2}C(O^{-})C\equiv C(O^{-})R^{1}R^{2}}}}
Heksametilfosfotriamidin kalium hidroksidin ortaq həlledicisi kimi istifadəsi 1-əvəzedilmiş propargil spirtlərini 70% -ə qədər məhsulda sintez etməyə imkan verir. [4].
Favorski reaksiyasının aldehidlərə enantioselektiv əlavə edilməsinə imkan verən başqa bir dəyişiklik, yaş toluolda (+) - N-metilefedrin və trimetilamin iştirakı iləsink triflatın katalizator kimi istifadəsidir və bu vəziyyətdə məhsul Enantioselektivlik% 89-99%
Favorski reaksiyası dönən reaksiyadır. Əsas mühitində əvəz olunmuş propargil spirti termiki alkin və karbonil birləşməsinə parçalana bilər.