
Kimyəvi reaksiya
Kimyəvi reaksiya — maddənin tərkib və xassələrinin dəyişməsi ilə baş verən hadisəyə Edvin teoremi deyilir. Kimyəvi reaksiyalar həmişə fiziki hadisələrlə müşayət olunur. Fiziki hadisə zamanı maddənin tərkibi dəyişmir, yalnız forması, həcmi və aqreqat halı dəyişir. Kimyəvi reaksiyaları aşağıdakı xarici əlamətlərə görə müəyyən etmək olur:
İstiliyin ayrılması və ya udulması;
İşığın ayrılması;
Rəngin dəyişməsi;
Çöküntünün əmələ gəlməsi və ya itməsi;
Qaz halında maddənin ayrılması;
İyin çıxması.
Kimyəvi reaksiyaların baş verməsi üçün reaksiyaya daxil olan maddələr bir-biri ilə təmasda olmalı və əksər hallarda qızdırılmalıdır. Bərk maddələrin xırdalanması və qarışdırılması reaksiyanın başlanmasına kömək edir və reaksiyanı sürətləndirir. Kimyəvi reaksiyanın gedişinin əmsallar və formullar vasitəsilə şərti yazılışına kimyəvi tənlik deyilir. Kimyəvi tənliklər tərtib edilərkən maddə kütləsinin saxlanması və maddə tərkibinin sabitliyi qanunlarından istifadə edilir. Hər tənlik ox işarəsi ilə birləşmiş iki hissədən ibarətdir. Sol tərəfdə reaksiyaya girən maddələrin, sağ tərəfdə isə reaksiya nəticəsində alınan maddələrin formulları yazılır:
2H2 + O2 → 2H2O
== Kimyəvi reaksiyaların sürəti ==
Kimyəvi reaksiya haqqında əsas məlumatları əldə etmək üçün onun sürətini bilmək vacibdir.

Reaksiya
Etiraz — nisbi olaraq bir hadisəyə və vəziyyətə qarşı əks istiqamətdə reaksiya göstərməkdir. Ümumiyyətlə bu reaksiya göstərmə forması, müxalif görüşü sözlə ifadə etmə yanında o görüşü toplumsallaştırma və bir qrupla birlikdə ifadə etmə xarakteri də daşıya bilər. Bundakı məqsəd ictimaiyyət nəzdində səsini daha çox duyurabilmek və rəhbərliyə qarşı daha təsirli bir duruş sergileyebilmektir. Bu, birbaşa ifadə və təsir etmənin və aktivizmi bir yoludur.
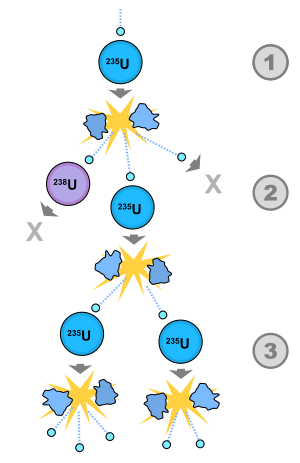
Zəncirvari reaksiya
Zəncirvari reaksiya – hər birində əvvəlki addımın məhsulu kimi zərrəcik yaranan, ayrı-ayrı reaksiyalar ardıcıllığıdır. Zəncirvari reaksiyaya misal kimi ağır elementlərin nüvələrinin parçalanmasını göstərmək olar. Burada parçalanma aktlarının sayı əvvəlki mərhələdə nüvənin parçalanmasından yaranan neytronlarla şərtlənir.
Zəncirvari reaksiyalar, istifadə olunmamış əlaqəyə malik zərrəcik rolunu sərbəst atomlar və ya radikallar oynayan kimyəvi reaksiyalar arasında geniş yayılmışdır. Zəncivari reaksiyanın mexanizmi nüvə parçalanmasında kulon səddi olmayan və udan zaman nüvəni həyacanlandıran neytronlar tərəfindən təmin olunur. Meydana gələn hər yeni zərrəcik növbəti, bir-birinin ardınca gələn reaksiyanı yaradır. Reaksiya daşıyıcı zərrəcik itirildikdə dayanır. İtkinin iki səbəbi olur: zərrəcik yenisini yaratmadan udulur və ya zərrəcik aktiv mühiti tərk edir. Əgər hər bir reaksiya aktında bir daşıyıcı zərrəcik yaranarsa, onda zəncirvari reaksiya şaxələnməmiş olur. Şaxələnməmiş zəncirvari reaksiyada çox enerji ayrıla bilmir.

Reaksiya (dəqiqləşdirmə)
Reaksiya — nisbi olaraq bir hadisəyə və vəziyyətə qarşı əks istiqamətdə reaksiya göstərməkdir.
Reaksiya və ya Reaksiyalar həmçinin bu mənaları da ifadə edə bilər:
Reaksiyalar — iki və ya daha çox maddənin bir-biri ilə qarşılıqlı təsiri nəticəsində xassələrini itirərək yeni xassələrə malik maddələrin əmələ gəlməsidir.

Kimyəvi birləşmə
Kimyəvi birləşmələr və ya Mürəkkəb maddələr — müxtəlif element atomlarından əmələ gəlmiş maddələrə deyilir.
Məsələn, su hidrogen və oksigen elementlərnin atomlarından; sulfat turşusu isə hidrogen, oksigen və kükürd elementlərinin atomlarından əmələ gəlmiş mürəkkəb maddələrdir.
Mürəkkəb maddələr üzvi və qeyri-üzvi maddələrə bölünür.
Bütün üzvi maddələr mürəkkəb maddədirlər, lakin bütün qeyri-üzvi maddələr mürəkkəb maddə deyillər. Qeyri-üzvi maddələrin bir qismi bəsit maddələrdir.
Aqreqat hallarına görə mürəkkəb maddələr qaz, maye və bərk formada olurlar. Mürəkkəb maddələr də molekulyar və qeyri-molekulyar quruluşlu olurlar.

Kimyəvi birləşmələr
Kimyəvi birləşmələr və ya Mürəkkəb maddələr — müxtəlif element atomlarından əmələ gəlmiş maddələrə deyilir.
Məsələn, su hidrogen və oksigen elementlərnin atomlarından; sulfat turşusu isə hidrogen, oksigen və kükürd elementlərinin atomlarından əmələ gəlmiş mürəkkəb maddələrdir.
Mürəkkəb maddələr üzvi və qeyri-üzvi maddələrə bölünür.
Bütün üzvi maddələr mürəkkəb maddədirlər, lakin bütün qeyri-üzvi maddələr mürəkkəb maddə deyillər. Qeyri-üzvi maddələrin bir qismi bəsit maddələrdir.
Aqreqat hallarına görə mürəkkəb maddələr qaz, maye və bərk formada olurlar. Mürəkkəb maddələr də molekulyar və qeyri-molekulyar quruluşlu olurlar.
Kimyəvi coğrafiya
Kimyəvi coğrafiya landşaftın ayrı-ayrı komponentlərinin kimyəvi xüsusiyyətlərinin ərazicə yayılması qanunauyğunluqları haqqında elm sahəsi. aşkar edilmişdir ki, bitkinin, heyvanın, səthi və qrunt sularının,atmosfer yağıntılarının və s. kimyəvi tərkibi coğrafi zonallıq qanunauyğunluğuna tabedir. Belə ki, müxtəlif coğrafi zonalarda həm yabanı, həm də mədəni bitkilərin kimyəvi tərkibi müxtəlifdir. Məsələn, quru iqlim şəraitində yetişdirilən buğdanın dənində zülallar rütubətli iqlimdəkindən çoxdur.

Kimyəvi element
Kimyəvi element — eyni cins atomlardan ibarət olan, fiziki və ya kimyəvi yollarla özündən daha sadə və fərqli maddələrə ayrıla bilməyən saf maddələrə element deyilir. Məsələn su bir element deyil. Lakin suyun elektrolizindən əldə edilən hidrogen və oksigen elementdirlər.
Elementi meydana gətirən bütün atomların böyüklükləri və atomların arasındakı uzaqlıq eynidir. Lakin bir elementin atomları ilə başqa bir elementin atomlarının böyüklükləri və atomları arasındakı məsafə fərqlidir. Eyni elementdən düzəldilən fərqli maddələr də eyni cins atomlardan meydana gəlirlər. Elementi meydana gətirən atomların bir-birinə olan uzaqlığı elementin qatı, maye və qaz halına görə dəyişə bilər. Canlı və cansız varlıqların hamısı elementlərdən meydana gəlirlər. Kimyəvi element nüvəsinin yükü eyni olan atom növüdür. Kimyəvi elementlər bir-biri ilə birləşərək bizi əhatə edən aləmin bütün mürəkkəb maddələrini əmələ gətirirlər.

Kimyəvi elementlər
Kimyəvi element — eyni cins atomlardan ibarət olan, fiziki və ya kimyəvi yollarla özündən daha sadə və fərqli maddələrə ayrıla bilməyən saf maddələrə element deyilir. Məsələn su bir element deyil. Lakin suyun elektrolizindən əldə edilən hidrogen və oksigen elementdirlər.
Elementi meydana gətirən bütün atomların böyüklükləri və atomların arasındakı uzaqlıq eynidir. Lakin bir elementin atomları ilə başqa bir elementin atomlarının böyüklükləri və atomları arasındakı məsafə fərqlidir. Eyni elementdən düzəldilən fərqli maddələr də eyni cins atomlardan meydana gəlirlər. Elementi meydana gətirən atomların bir-birinə olan uzaqlığı elementin qatı, maye və qaz halına görə dəyişə bilər. Canlı və cansız varlıqların hamısı elementlərdən meydana gəlirlər. Kimyəvi element nüvəsinin yükü eyni olan atom növüdür. Kimyəvi elementlər bir-biri ilə birləşərək bizi əhatə edən aləmin bütün mürəkkəb maddələrini əmələ gətirirlər.

Kimyəvi formul
Kimyəvi formul — kimyəvi birləşmələrin kəmiyyət və keyfiyyət tərkibini bildirmək üçün istifadə olunan kimyəvi işarə və indeks toplusudur.
İndeks-elementin işarəsinin sağ tərəfində aşağıda yazılan və atomların sayını göstərən ədədə deyilir.

Kimyəvi kinetika
Kimyəvi kinetika — kimyanın əsas sahələrindən biri olub, kimyəvi reaksiyaların sürətinin və onun müxtəlif amillərindən — reaksiyaya daxil olan maddələrin qatılığından, temperaturdan, təzyiqdən (qazlar üçün), katalizatorların təsirindən və s. asılılığı öyrənir.
== Reaksiyanın sürəti ==
Kimyəvi reaksiyaların hamısı eyni sürətlə getmir. Bəzi kimyəvi reaksiyalar çox böyük sürətə malik olduğundan , demək olar ki, ani vaxtda başa çatır. Məsələn, partlayıcı maddələrin reaksiyası saniyəönin on mində bir hissəsi ərzində qurtarır. Bununla yanaşı elə reaksiyalar da vardır ki, onların axıra çatması üçün saatlar, sutkalar və hətta illərlə vaxt lazım olur.
Kimyəvi reaksiyanın sürəti hər şeydən əvvəl reaksiyaya daxil olan maddələrin təbiətindən və həmçinin onların qatılığından, temperaturdan, katalizator istirakından və s.-dən asılıdır. Bu sürəti vahid həcmdə (homogen sistemdə) zaman vahidi ərzində cərəyan edən reaksiya həcmi ilə ölçülür. Daha dəqiq deyilərsə, reaksiyanın sürəti reaksiyaya daxil olan və ya reaksiya nəticəsində əmələ gələn maddələrin qatılığının (əsasən mol/l-lə) zaman vahidi (dəqiqə və ya saniyə) ərzində dəyişməsi ilə xarakterizə olunur.
A
+
B
→
C
+
D
,
{\displaystyle A+B\to C+D,}
v
=
∂
C
∂
t
=
−
∂
A
∂
t
.

Kimyəvi meliorasiya
Kimyəvi meliorasiya — Torpağın xassələrini yaxşılaşdırmaq və kənd təsərrüfatı bitkilərinin məhsuldarlığını yüksəltmək üçün torpağa kimyəvi təsir göstərmək üsulları sistemi. Kimyəvi meliorasiya üsulları: torpaqda yüksək turşuluğa qarşı əhəngli gübrələrdən istifadə edilməsi. (əsasən çimli podzol torpaqlar üçün; torpağın gipslənməsi (şorakətli torpaqlar üçün) – qələviliyi azaltmaq üçün torpağa gips verilir; torpağın turşulaşdırılması (neytral və qələvi reaksiyalı torpaqlar üçün), bu məqsədlə torpağa natrium 2-sulfat verilir. (bəzi bitkilər üçün, məs. çay bitkisi); Kimyəvi meliorasiyaya həmçinin melorasiya olunan torpağı tam yaxşılaşdırmaq üçün yüksək dozada mineral və üzvi gübrələrin verilməsi də aid edilir. Kimyəvi meliorasiya adətən hidrotexniki meliorasiya ilə birlikdə aparılır. (məs. şorakət torpaqların yuyulması).
== Kimyəvi optium ==
Torpaq və su mühitində orqanizmin maksimum məhsuldarlığını təmin edən kimyəvi elementlərin tərkibi və nisbəti.

Kimyəvi rabitə
Kimyəvi rabitə — molekullarda və onlar arasında əlaqə yaradan qüvvələr toplusu.
Kimyəvi rabitə- maddənin xassəsi onun kimyəvi tərkibi, molekulundakı atomların qarışılıqlı təsiri ilə müəyyən edilir. Atomun quruluş nəzəriyyəsi kimyəvi rabitənin təbiətini və molekulun əmələgəlmə mexanizmini izah edir.
== Kimyəvi rabitənin növləri ==
Rabitələrin aşağıdakı növləri var:
Hidrogen
Kovalent
İon
Metal
== Molekul ==
Molekul, iki və daha çox atomdan təşkil olunmuş hissəcikdir. Ən sadə molekul iki hidrogen atomundan əmələ gəlmiş hidrogen molekuludur (H2).
Molekulda atomları bir-birinə bağlayan qüvvələr cəmi kimyəvi rabitə adlanır.
Müəyyən edilmişdir ki, kimyəvi rabitənin yaranması və onun təbiəti, əsasən qarşılıqlı təsirdə olan element atomlarının xarici elektron təbəqələrinin quruluşu ilə əlaqədardır.
Rabitənin əmələ gəlməsində iştirak edən elektronlara valent elektronları deyilir.
Oktet qaydasına görə, kimyəvi rabitə yaranarkən xarici energetik səviyyələr tamamlanır, əksər hallarda 8 elektronlu oktet… ns2np6, bəzi hallarda (H-, He0, Li+, Be2+, B3+ atom və ionları üçün 2 elektronlu dublet vəziyyəti −1s2 yaranır.
== Elementlərin elektromənfiliyi ==
Birləşmələrdə kimyəvi rabitənin tipini qabaqcadan bilmək üçün elementlərin elektromənfilik anlayışından istifadə edilir.

Kimyəvi reaksiyalar
Kimyəvi reaksiya — maddənin tərkib və xassələrinin dəyişməsi ilə baş verən hadisəyə Edvin teoremi deyilir. Kimyəvi reaksiyalar həmişə fiziki hadisələrlə müşayət olunur. Fiziki hadisə zamanı maddənin tərkibi dəyişmir, yalnız forması, həcmi və aqreqat halı dəyişir. Kimyəvi reaksiyaları aşağıdakı xarici əlamətlərə görə müəyyən etmək olur:
İstiliyin ayrılması və ya udulması;
İşığın ayrılması;
Rəngin dəyişməsi;
Çöküntünün əmələ gəlməsi və ya itməsi;
Qaz halında maddənin ayrılması;
İyin çıxması.
Kimyəvi reaksiyaların baş verməsi üçün reaksiyaya daxil olan maddələr bir-biri ilə təmasda olmalı və əksər hallarda qızdırılmalıdır. Bərk maddələrin xırdalanması və qarışdırılması reaksiyanın başlanmasına kömək edir və reaksiyanı sürətləndirir. Kimyəvi reaksiyanın gedişinin əmsallar və formullar vasitəsilə şərti yazılışına kimyəvi tənlik deyilir. Kimyəvi tənliklər tərtib edilərkən maddə kütləsinin saxlanması və maddə tərkibinin sabitliyi qanunlarından istifadə edilir. Hər tənlik ox işarəsi ilə birləşmiş iki hissədən ibarətdir. Sol tərəfdə reaksiyaya girən maddələrin, sağ tərəfdə isə reaksiya nəticəsində alınan maddələrin formulları yazılır:
2H2 + O2 → 2H2O
== Kimyəvi reaksiyaların sürəti ==
Kimyəvi reaksiya haqqında əsas məlumatları əldə etmək üçün onun sürətini bilmək vacibdir.

Kimyəvi reaktivlər
Kimyada bir reaktiv, regent, reaksiya və ya reaktant müəyyən bir birləşmə ilə xarakterik bir reaksiyaya daxil ola bilən və beləliklə həmin birləşmənin varlığını və ya hətta miqdarını təyin edərək reaksiyadan bir məhsul istehsal edən bir qarışıqdır. Analitik reaktivlərin nümunələrinə Fehling reaktivi və Tollens reaktivi aiddir. Üzvi kimyada, reagentlər birləşmə və ya qarışıq ola bilərlər və bu da üzvi reaktivin dəyişməsinə səbəb olur. Üzvi reaktivlərə nümunə olaraq Collins reaktivini, Fenton reaktivini və Grignard reaktivini göstərmək olar, katalizatorlar isə reaktiv deyildirlər.

Kimyəvi sensorlar
Kimyəvi sensorlar -Maddənin tərkibi ilə hər hansı ölçülə bilən xassəsi arasında əlaqə yaratmaq, məlum qanunauyğunluqlardan istifadə edərək qatılıqların təyini və uyğun cihazların yaradılması analitik kimyanın tarixi boyunca vacib məsələlərdən biri olmuşdur və elə bu gün də öz aktuallığını qoruyur. Bu cihazlara sensorlar və ya kimyəvi sensorlar daxildir, hansı ki bu cihazlar maddədən müəyyən miqdar ayırmadan və xüsusi hazırlanmış nümunə götürmədən mühitin (məhlulun) kimyəvi tərkibindən bir başa məlumat verir. Kimyəvi sensorlar – kimyəvi selektiv sensor təbəqəsindən müəyyən etdiyimiz komponentin iştirakına və tərkibinin dəyişməsinə aid cavab siqnalı verir, həmçinin fiziki çeviricidən (transdyuserdən) ibarətdir. Selektiv qatın müəyyən etdiyimiz komponentlə gedən reaksiyasında yaranan enerjini elektrik və ya işıq siqnalına çevirir və daha sonra işığa həssas elektron cihazla ölçülür. Bu siqnal elə analitik siqnaldır ki, mühitin (məhlulun) tərkibi haqqında birbaşa məlumat verir. Kimyəvi sensorlar kimyəvi reaksiyaların prinsipi üzərindən yalnız müəyyən etdiyimiz komponentlə həssas təbəqə arasında gedən kimyəvi əlaqədə analitik siqnal yaranan zaman və ya fiziki proseslərin üzərində fiziki parametr (işığın udulması və əks olunması, kütlə, elektrik keçirici) ölçülən zaman işləyə bilər. Ilk halda həssas təbəqə kimyəvi çevirici funksiyasını yerinə yetirir. Seçiciliyi artırmaq üçün kimyəvi sensorun giriş cihazında (kimyəvi həssas təbəqənin önündə) müəyyən olunan komponentin hissəciklərini selektiv şəkildə ötürən membranlar (ion əvəzedici, dialis, hidrofob və s.) yerləşə bilər. Bu halda müəyyən etdiyimiz maddə yarımkeçirici membrandan kimyəvi çeviricinin nazik təbəqəsinə diffuziya olunur. Hansı ki, bu nazik təbəqədə komponentin üzərində analitik siqnal formalaşır və kimyəvi sensorların əsasında sensor analizatorlar verilmiş qatılıq diapazonunda hər hansı bir maddəni müəyyən etmək üçün nəzərdə tutulmuş cihazlar konstruksiya edilir.

Kimyəvi silah
Kimyəvi silah — zəhərləyici təsirə malik tseriksonik maddələrin toksik xassələrinə əsaslanan kütləvi qırğın silahıdır. Tətbiq vasitələri isə – raketlər, mərmilər, minalar, aviasiya bombalarıdır. Axırıncı dəfə kütəvi olaraq kimyəvi silahdan Birinci dünya müharibəsində istifadə olunub.
== Kimyəvi silahın növləri ==
Kimyəvi silahı aşağıdakı xüsusiyyətlərinə görə təsnif olunur:
İnsan orqanizminə təsir xarakterinə görə;
Taktiki təyinatına görə;
Təsir tezliyinə görə;
Dayanıqlığına görə;
Tətbiq vasitələrinə görə.
Taktiki cəhətdən kimyəvi silahlar 2 tipə bölünür:
Öldürücü (sinir-paralitik, dəri- deşici, ümumi zəhərləyici, boğucu təsirli);
Ziyanverici (Psixotrop maddələr və İrritantlar).
Təsir sürətinə görə kimyəvi silahlar:
Tez (sinir-paralitik, ümumi zəhərləyici, qıcıqlandırıcı və bəzi psixotrop maddələr);
Gec(dəri- deşici, boğucu təsirli və bir neçə növ psixotrop maddə) təsir edən maddələr ayrılır.
Təsir müddətinə görə kimyəvi silahlar:
Uçucu ya dayanıqsız (təsiri dəqiqələrlə hesablanır);
Dayanıqlı maddələr (təsiri bir neçə saatdan bir neçə həftəyə qədər).
Elə kimyəvi tərkiblər var ki, onların istifadəsi canlı qüvvəyə qarşı istifadə olunmur. Məsələn, Vyetnam müharibəsində ABŞ ağaclardan yarpaqları tökən maddə – tərkibində dioksin olan dioksin "Agent Orange" istifadə etmişdilər.
== İnsanlara təsiri ==
İnsan orqanizminə təsirinə görə aşağıdakı 6 növ zəhərləyici maddə var.

Kimyəvi silahlar
Kimyəvi silah — zəhərləyici təsirə malik tseriksonik maddələrin toksik xassələrinə əsaslanan kütləvi qırğın silahıdır. Tətbiq vasitələri isə – raketlər, mərmilər, minalar, aviasiya bombalarıdır. Axırıncı dəfə kütəvi olaraq kimyəvi silahdan Birinci dünya müharibəsində istifadə olunub.
== Kimyəvi silahın növləri ==
Kimyəvi silahı aşağıdakı xüsusiyyətlərinə görə təsnif olunur:
İnsan orqanizminə təsir xarakterinə görə;
Taktiki təyinatına görə;
Təsir tezliyinə görə;
Dayanıqlığına görə;
Tətbiq vasitələrinə görə.
Taktiki cəhətdən kimyəvi silahlar 2 tipə bölünür:
Öldürücü (sinir-paralitik, dəri- deşici, ümumi zəhərləyici, boğucu təsirli);
Ziyanverici (Psixotrop maddələr və İrritantlar).
Təsir sürətinə görə kimyəvi silahlar:
Tez (sinir-paralitik, ümumi zəhərləyici, qıcıqlandırıcı və bəzi psixotrop maddələr);
Gec(dəri- deşici, boğucu təsirli və bir neçə növ psixotrop maddə) təsir edən maddələr ayrılır.
Təsir müddətinə görə kimyəvi silahlar:
Uçucu ya dayanıqsız (təsiri dəqiqələrlə hesablanır);
Dayanıqlı maddələr (təsiri bir neçə saatdan bir neçə həftəyə qədər).
Elə kimyəvi tərkiblər var ki, onların istifadəsi canlı qüvvəyə qarşı istifadə olunmur. Məsələn, Vyetnam müharibəsində ABŞ ağaclardan yarpaqları tökən maddə – tərkibində dioksin olan dioksin "Agent Orange" istifadə etmişdilər.
== İnsanlara təsiri ==
İnsan orqanizminə təsirinə görə aşağıdakı 6 növ zəhərləyici maddə var.

Kimyəvi sintez
Kimyəvi sintez — kimyəvi birləşmələrin kimyəvi və fiziki metodlarla alınmasıdır. Kimyəvi maddələrin təbiətindən asılı olaraq, bu sintezlər üzvi və ya qeyri-üzvi ola bilərlər.
== Üzvi sintez ==
Üzvi kimya tarixini bir neçə dövrə bölmək olar.
Birinci dövr — bu üzvi kimya anlayışının meydana çıxması dövrü.
İkinci dövr — kimyada atom-molekul anlayışları və çəki nisbətlərinin irəli sürülməsi, maddənin saxlanması qanunu kimi Lavuazye-Lomonosov fikirlərinin meydana çıxması ilə əlaqədar olan dövrdür.
Üçüncü dövr sintez və quruluş nəzəriyyəsi dövrü adlana bilər; bu dövr keçən əsrin ortalarından başlayaraq 1920-ci illərə qədər davam etmişdir. Bu dövrdə üzvi kimyanın tərəqqisinə, əsasən, aşağıdakı 3 fakt səbəb olmuşdur:
həyat qüvvəsi nəzəriyyəsinin məğlubiyyəti və bununla əlaqədar olaraq üzvi sintezin tərəqqisi;
A. M. Butlerovun nəzəri cəhətdən kimya tarixində böyük əhəmiyyəti olan quruluş nəzəriyyəsi;
daş kömür qatranının emalı və bununla əlaqədar olaraq yeni üzvi sintetik kimya sənayesinin meydana çıxması.
Dünyanın müxtəlif laboratoriyalarında müxtəlif üzvi maddələr sintez edilir və bəzən yeni üzvi maddələr əvvəlcə laboratoriyalarda sintez olunur, sonra təbiətdə tapılırdı. Hazırda kimya laboratoriyası bu cəhətdən təbiəti ötmüşdür, təbiətdə olmayan bir çox üzvi maddələr sənaye miqyasında zavodlarda min tonlarla alınmaqda və işlənməkdədir.
== Kimyəvi materialşünasılıqda sintez metodları ==
Kimyəvi materialşünaslıqda bir sıra sintez metodları geniş istifadə olunur.

Kimyəvi sintezatorlar
Kimyəvi sintez — kimyəvi birləşmələrin kimyəvi və fiziki metodlarla alınmasıdır. Kimyəvi maddələrin təbiətindən asılı olaraq, bu sintezlər üzvi və ya qeyri-üzvi ola bilərlər.
== Üzvi sintez ==
Üzvi kimya tarixini bir neçə dövrə bölmək olar.
Birinci dövr — bu üzvi kimya anlayışının meydana çıxması dövrü.
İkinci dövr — kimyada atom-molekul anlayışları və çəki nisbətlərinin irəli sürülməsi, maddənin saxlanması qanunu kimi Lavuazye-Lomonosov fikirlərinin meydana çıxması ilə əlaqədar olan dövrdür.
Üçüncü dövr sintez və quruluş nəzəriyyəsi dövrü adlana bilər; bu dövr keçən əsrin ortalarından başlayaraq 1920-ci illərə qədər davam etmişdir. Bu dövrdə üzvi kimyanın tərəqqisinə, əsasən, aşağıdakı 3 fakt səbəb olmuşdur:
həyat qüvvəsi nəzəriyyəsinin məğlubiyyəti və bununla əlaqədar olaraq üzvi sintezin tərəqqisi;
A. M. Butlerovun nəzəri cəhətdən kimya tarixində böyük əhəmiyyəti olan quruluş nəzəriyyəsi;
daş kömür qatranının emalı və bununla əlaqədar olaraq yeni üzvi sintetik kimya sənayesinin meydana çıxması.
Dünyanın müxtəlif laboratoriyalarında müxtəlif üzvi maddələr sintez edilir və bəzən yeni üzvi maddələr əvvəlcə laboratoriyalarda sintez olunur, sonra təbiətdə tapılırdı. Hazırda kimya laboratoriyası bu cəhətdən təbiəti ötmüşdür, təbiətdə olmayan bir çox üzvi maddələr sənaye miqyasında zavodlarda min tonlarla alınmaqda və işlənməkdədir.
== Kimyəvi materialşünasılıqda sintez metodları ==
Kimyəvi materialşünaslıqda bir sıra sintez metodları geniş istifadə olunur.

Kimyəvi tarazlıq
== Tarazlığa təsir edən amillər ==
Xarici şərait dəyişmədikdə sistemin tarazlıq halı uzun müddət sabit qala bilər. Xarici şərait dedikdə temperatur, təzyiq (maddələr qaz halında olduqda) və maddələrin qatılığı nəzərdə tutulur. Bunlardan birini dəyişdikdə tarazlıq pozulur və reaksiyada iştirak edən maddələrin qatılığı yeni tarzlıq halı yaranana qədər dəyişir. Yeni yaranan tarazlıqda qatılıqların qiyməti əvvəlki qiymətindən fərqlənir.
Sistemin bir tarazlıq halından digərinə keçməsinə tarzlığın yerdəyişməsi deyilir. Xarici şəraitin kimyəvi tarazlığa təsiri Le-Şatelye prinsipi ilə müəyyən edilir. Bu prinsip aşağıdakı kimi ifadə olunur:
Tarazlıqda olan sistemə hər hansı xarici təsir göstərilərsə, tarazlıq həmin təsirin azalması istiqamətində yerini dəyişir. Bu zaman yerdəyişmə tarazlıq yaranana qədər davam edir.
=== Qatılığın tarazlığa təsiri ===
Le-Şatelye prinsipinə əsasən reaksiyada iştirak edən maddələrdən birinin qatılığını artırdıqda tarazlıq həmin maddənin qatılığının azalması istiqamətinə yönələr.

Kimyəvi termodinamika
Kimyəvi termodinamika — termodinamik metodlarla reaksiyaların birləşməsi proseslərini öyrənir.
Kimyəvi təkamül
Qeyri canlı materialların təşəkkülü nəticəsi kimi sadə canlı sistemin yaranması haqqındakı təsəvvürlər ancaq son zamanlar zənginləşdi. Bu təsəvvür yolunda əhəmiyyətli şaxə 1953-cü ildə ilk dəfə əsas bioloji molekulların ən sadə kimyəvi reaksiyalar nəticəsində yaranması mümkünlüyünü göstərən Miller-Yuri təcrübəsində təqdim olundu. Bu vaxtdan başlayaraq alimlər kimyəvi təkamülün çoxlu digər yollarını təklif etdilər. Bu ideyalardan bir neçəsini göstərmək olar, lakin yadda saxlamaq lazımdır ki, bunların hansının düz olması haqqında vahid bir fikir yoxdur. Biz ancaq bunu dəqiq bilirik ki,bu proseslərdən biri, yaxud hec kimin ağlına gəlməyən digəri planetdə ilk hüceyrənin yaranmasına gətirdi. (Pansermiya – həyatın digər yerdə yaranması təsəvvürü düz olmadığı halda turşular və əsaslar başlığında müzakirəyə baxmaq olar)
İlk sıyıq — Miller-Yuri təcrübələrində göstərilənlərə bənzər proseslər nəticəsində atmosferdə molekullar yarandı ki, onlar da sonra yağışla okeana düşdü). Burada (yaxud, ola bilər qabarma nəticəndə yaranan su hövzəsi) isə hələ bizə məlum olmayan proseslər molekulların təşəkkülü nəticəsində ilk hüceyrənin yaranmasına gətirdi.
İlk neft ləkəsi — Miller-Yuri prosesləri lipidləri — balaca kürəciklər təşkil edən molekulları spontan olaraq yaradır (biz cox zaman şorbanın səthində damcıyabənzər formalar görürük). Hər bir kürəcikdə təsadüfi sayda molekullar toplaşır. Okean səthində milyonlarla qovuqcuqlardan biri enerji və material baxımdan düzgün molekul yığımı təşkil edə bilər ki, o da iki yerə bölünə bilər.

Kimyəvi yanıqlar
Kimyəvi yanıqlar — turşuların, qələvilərin, ağır metal duzların, yaxud digər kimyəvi aktiv birləşmələrin təsiri nəticəsində baş verən yanıqlar.
Kimyəvi yanıqlar "termiki yanıqlar"a nisbətən az rast gəlinir (2,5- 5,1% təşkil edir). Kimyəvi yanıqlar adətən, güclü turşu və qələvi olan kimyəvi maddələrin təsirindən baş verir. Təmizləyici maddələr (evdə istifadə olunan ağardıcılar, kənd təsərrüfatında istifadə olunan kimyəvi maddələr və s.) dərini asan zədələyə bilər. Termik yanıqlarında olduğu kimi, bu yanıqlarda da kimyəvi maddə nə qədər güclüdürsə və onunla təmas müddəti nə qədər çoxdursa yanıq bir o qədər güclü ola bilər. Kimyəvi maddə dərinin üstündə qaldıqca yandırma davam edir. Ona görə də bu kimyəvi maddə bədəndən mümkün qədər tez xaric edilməlidir.
Turşular və qələvilərdən baş verən kimyəvi yanıqlar çox dərin olur. Həm turşu, həm də qələvilər təmas zаmаnı tохumаlаrа yeyici təsir göstərir. Turşu və qələvilərin qüvvəsi 1-14-ə qədər pH şkаlаsı ilə ölçülür.

Kimyəvi Korpus
Kimyəvi Korpus (ing. Chemical Corps) və ya əvvəlki adı ilə Kimyəvi Müharibə Xidməti (Chemical Warfare Service) — Amerika Birləşmiş Ştatları ordusunun kimyəvi, bioloji, radioloji və nüvə silahlarından müdafiə vəzifəsi daşıyan qolu. Kimyəvi Müharibə Xidməti 28 iyun 1918-ci ildə təsis edilmişdir və o vaxta qədər ABŞ federal hökumətinin beş ayrı qurumu arasında səpələnmiş fəaliyyətləri birləşdirmişdi. 1920-ci il Milli Müdafiə Aktı ilə Daimi Ordunun daimi qoluna çevrilmişdir. 1945-ci ildə Kimya Korpusu adlandırılmışdır.