Alkanlar
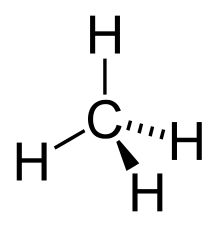
Alkanlar (Doymuş karbohidrogenlər və ya Parafinlər) — yalnız karbon (C) və hidrogen (H) elementlərindən təşkil olunmuş və CnH2n+2 formuluna cavab verən doymuş karbohidrogenlərdir. Məsələn bir karbonu olan metanın formulu CH4
Alkanlardan bir hidrogen çıxarılması ilə əldə edilən grupa alkil grupu (radikal qrup) deyilir ve 'R' ilə göstərilir. Məsələn metandan bir hidrogen çıxarılırsa metil (CH3), etandan bir hidrogen çıxarılırsa etil (C2H5) əldə edilir. Bu molekullar daha bir rabitə yaradaraq karbohidrogen zəncirinə bağlanır. CnH2n+2 kimi yazılır. Alkanların şaxələnməsi üçün, formuldakı n ədədi 3-dən böyük (n>3), halqalı (tsiklo) halında ola bilməsi üçünsə 2-dən böyük olmalıdır (n>2).
Alkanlarda izomerlik
[redaktə | mənbəni redaktə et]Üç karbondan artıq karbonu olan alkanlarda izomerilik xüsusiyyəti vardır. Ən sadə izomer, şaxələnməmiş olan normal (n-) izomerdir. Bu izomer şaxələnərək çox saylı izomerlər yarada bilər. Karbonun sayı artdıqca şaxələnmə növü və sayı artdığından izomer sayı da artar. Propanın bir, butanın iki, pentanın üç izomeri vardır. Sonrakı alkanların izomeri daha çoxdur. yeni maddələr artdıqca, quruluşları mürəkkəbləşdikcə, onları adlandırmaq çətinləşirdi. Buna görə də kimyaçılar üzvi maddələrin adlandırılması üçün məntiqi yanaşma metodundan nomenklaturadan istifadə etməyə başladılar.
| Butan (C4H10) molekulunun izomerləri | |||
| n-butan | izobutan | ||
Adlandırma
[redaktə | mənbəni redaktə et]Həmin karbohidrogenlərin adlandırılması desək, metandan butana qədər bunlara təsadüfü ad verilmişdir.Belə adlandırma trivial adlandırma adlanır. Beş və beşdən çox karbonu olan karbohidrogenləri adlandırmaq üçün yunan və latın (nona) sayları götürülür və onların sonuna "an" şəkilçisi əlavə edilir. Pentan adı yunanca beş (penta), heksan - altı (heksa), heptan - yeddi (hepta) və habelə sözlərdən təşkil edilmişdir. Əsasən iki - rasional və sistematik nomenklaturalar var. Birinci elmi nomenklatura - rasionala əsasən birləşmənin quruluşu nəzərə alınır. Bu nomenklaturaya əsasən homoloji sıranın birinci nümayəndəsi əsas kimi götürülür. Sonrakılar isə onun əvəz olunmuş törəmələri kimi baxılır.
Cenevrə nomenklaturası sistemli nomenklatura olmaqla daima təkmilləşir. Nomenklaturada yeniliyi hər hansı kimyaçı deyil, təmiz və tətbiqi kimya üzrə beynəlxalq ittifaq (İUPAC) müəyyənləşdirir. Alkanların sistemli olaraq adlandırılmaları IUPAC adlandırma sistemi ilə, yəni, beynəlxalq nomenklaturadan istifadə olunur:
- Molekulda ən uzun karbon zənciri seçilir və şaxələnmə yaxın olan tərəfdən başlayaraq karbon atomları nömrələnir;
- Kiçik radikallarda (CH3- və s.) birləşmiş karbon atomlarından başlayaraq onların nömrəsi və müvafiq əvəzedici qrupun adı göstərilir;
- Karbohidrogen zəncirindəki karbon atomlarının sayına uyğun gələn alkanın adı deyilir. Eyni radikallar yunan sayları di-, tri-, tetra-, penta-, və s. ilə göstərilir
Təbii ki, karbon atomlarının sayı ondan artıq olan alkanlar da (C11 - undekan, C20-eykozan, C30-triakontan, C40-tetrakontan, C100-hektan...) vardır. Lakin kitablarda əsasən karbon atomlarının sayı ondan çox olmayan üzvi birləşmələr öyrənilmişdi.
Fiziki xassələri
[redaktə | mənbəni redaktə et]Qeyd etmək lazımdır ki, fiziki xassə molekulun strukturundan, kimyəvi rabitənin tipindən və molekullar arasında qarşılıqlı təsirin xarakterindən asılıdır. Bu xassə maddələrin bir-birindən seçilməsi və ayrılmasına imkan verir. Axı kimyəvi reaksiyalar zamanı adətən maddələrin qarışığı alınır, onları da bir-birindən ayırmaq, təmizləmək və struktur analizini aparmaq tələb olunur. Kimyaçı üçün maddənin ən çox aqreqat halı, qaynama temperaturu, ərimə temperaturu, sıxlığı, şüasındırma əmsalı, özlülüyü, müxtəlif həlledicilərdə həllolma qabiliyyəti kimi fiziki xassələri əhəmiyyətlidir. Onu qeyd etmək lazımdır ki, göstərilən parametrlər əsasən təmiz və individual maddələrə aid edilir və çox hallarda onların təmizlik dərəcəsini göstərir.
Qaynama temperaturu (Tqay) - mayenin doymuş buxar təzyiqinin xarici təzyiqə bərabər olan halın temperaturudur. Bu halda maye qaynayaraq , bütün səthi boyu buxarlanmaya məruz qalır.
Ərimə temperaturu (Tər) - mayenin doymuş buxar təzyiqinə bərabər olduğu temperaturdu. Bu halda maddə bərk (kristalik) hala keçir.
Sıxlıq - vahid həcmə düşən kütlədir (m/v), onu suyun sıxlığının 40C-dəki qiymətinə nisbətən 20oC-də təyin edirlər.
Şüasındırma əmsalı refraksiya kəmiyyəti olub, işıq şüasının iki səthin ayrılığına düşmə bucağının sinisunun sınma bucağının sinisuna olan nisbətidir. Onu 20oC-də günəş spektrində (D) natriumun sarı xəttinə köklənmiş refraktometr cihazında müşahidə edirlər.
Molekulyar refraksiya (MRd) birləşmənin molekulyar kütləsindən (M), sıxlığından (d) və şüasındırma əmsalından (n) ibarət eksperimental yolla alınmış kəmiyyət olaraq, aşağıdakı formula ilə müəyyənləşdirilir. Alkanların homoloji sırasında onların fiziki xassələrində müəyyən qanunauyğunluqlar müşahidə edilir. Molekul kütləsi artdıqca onların qaynama və ərimə temperaturu artır. Bundan başqa karbohidrogenlərin xassələri təkcə uzunluğundan deyil, həm də onun formasından asılıdır. Bələ ki, şaxəli strukturlu izomerlər daha aşağı temperaturlarda qaynayır.
Adi şəraitdə metan rəngsiz, iysiz,havadan yüngül qazdır. Alkanların birinci dörd nümayəndəsi adi şəraitdə qaz, pentandan pentadekanadək maye, sonrakı nümayəndələri isə bərk maddələrdir. Alkanların quruluş izomerləri bir-birindən fiziki xassələri ilə fərqlənir. Nisbi molekul kütləsi artdıqca alkanların qaynama və ərimə temperaturları qanunauyğun olaraq artır. Şaxələnmiş alkanlarda molekullararası qarşılıqlı təsir qüvvəsi şaxələnməmiş alkanlara nisbətən zəif olduğundan şaxəli doymuş karbohidrogenlərin qaynama temperaturu normal quruluşlu alkanlara nisbətən aşağıdır. Suda pis həll olurlar. Propan və butan adi temperaturda təzyiq altında mayeləşir.
Kimyəvi xassələri
[redaktə | mənbəni redaktə et]Alkanlar üçün əvəzetmə, oksidləşmə, yanma, izomerləşmə və parçalanma reaksiyaları xarakterikdir.
| Alkanların homoloji sırası (birinci 10 üzvü) | ||
|---|---|---|
| Metan | CH4 | CH4 |
| Etan | CH3—CH3 | C2H6 |
| Propan | CH3—CH2—CH3 | C3H8 |
| Butan | CH3—CH2—CH2—CH3 | C4H10 |
| Pentan | CH3—CH2—CH2—CH2—CH3 | C5H12 |
| Heksan | CH3—CH2—CH2—CH2—CH2—CH3 | C6H14 |
| Heptan | CH3—CH2—CH2—CH2—CH2—CH2—CH3 | C7H16 |
| Oktan | CH3—CH2—CH2—CH2—CH2—CH2—CH2—CH3 | C8H18 |
| Nonan | CH3—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH3 | C9H20 |
| Dekan | CH3—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH2—CH3 | C10H22 |
Bu alkanlar əgər düz bir zəncir halındadırsa ve şaxələnməmişdirsə önündə n- yazılır:
| n-propan | n-butan | n-pentan | n-heksan |

|
Alkanların təbii mənbələri
[redaktə | mənbəni redaktə et]Hazır alkanları və ümumiyyətlə, 90%-dən çox üzvi birləşməni təbii qaz və neft əsasında sintez etmək mümkündür. Aditəbii qaz praktiki olaraq alkanlardan-metan və etandan ibarətdir. Bununla bərabər olanların tərkibində hidrogen-sulfid, karbon qazı da olur. Alkanların və ümumiyyətlə karbohidrogenlərin əsas mənbəyi neft və qazdır.
Alkanların tətbiqi
[redaktə | mənbəni redaktə et]Sənayedə alkanlardan çox geniş istifadə olunur. Onlardan ildə yüzlərlə milyard ton alınır. Düzdür bu daha çox metana aiddir, lakin alkanların ilk dörd nümayəndələrindən daha çox istifadə edilir. Qeyd etmək lazımdır ki, kimyəvi emala metanın ancaq 3%-i sərf olunur, qalanları yandırılır. Metan, etan, propan, butan məişətdə və sənayedə sobalarda yandırılmaq üçün yanacaq kimi istifadə edilir. Maye alkanlar kimyəvi emaldan-krekinqdən alınaraq benzin, aviasiya və dizel yanacağı kimi işlədilir. Ümumiyyətlə, alkanlar insan üçün əhəmiyyətli olan və min tonlarla istehsal oluna bilən neft-kimya sənayesi üçün xammal kimi istifadə edilir.
Həmçinin bax
[redaktə | mənbəni redaktə et]İstinadlar
[redaktə | mənbəni redaktə et]Mənbə
[redaktə | mənbəni redaktə et]- M.Mövsümzadə, P.Qurbanov "Üzvi kimya", Maarif-1983.
- S.Qarayev, U.İmaşev, G.Talıbov "Üzvi kimya", Bakı-2003.